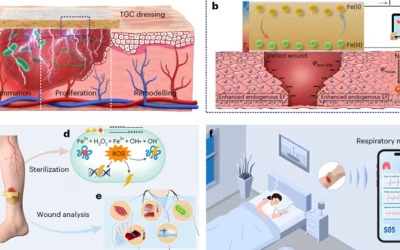
近日,新加坡国立大学(NUS)健康创新与技术研究所(iHealthtech)的研究团队在弗朗科-奥布雷贡副教授和亚历克斯·泰博士的带领下,发现了一种利用脉冲电磁场激活肌肉细胞天然抗癌防御机制的新方法。

第一作者:Yee Kit Tai
通讯作者:Yee Kit Tai, Alfredo Franco-Obregón
DOI:10.3390/cells13050460
这项突破性的研究展示了通过简短而温和的脉冲电磁场暴露,可以刺激肌肉细胞产生并释放具有抗癌特性的蛋白质。
这些可溶性蛋白质能够抑制乳腺癌细胞的生长、侵袭和迁移,表现出与运动类似的抗癌效果。
即利用具有特殊特征的短暂而温和的脉冲电磁脉冲来刺激肌肉细胞产生和释放具有抗癌特性的蛋白质。

新加坡国立大学健康创新与技术研究所的
副教授 Alfredo Franco-Obregón(左)和 Alex Tai 博士(右)
创新疗法
具体来说,研究团队发现,10分钟的低幅度脉冲电磁场暴露(1.5 mT)可以生成一种条件培养基(pCM),这种培养基能够显著抑制乳腺癌细胞的生长和迁移。
这一无药物、非侵入性的疗法为未来癌症治疗和癌症生物标志物的发现开辟了新的道路。
研究团队表示,这一方法不仅有望提供新的癌症治疗手段,还可能为癌症预防和早期诊断带来新的希望。
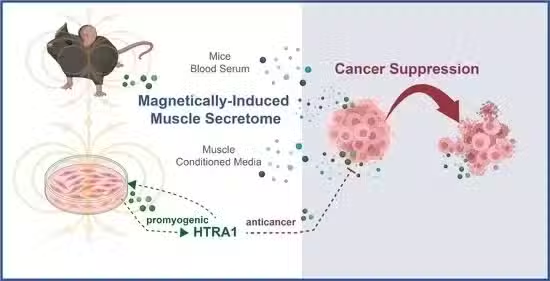
图形概要
HTRA1蛋白的作用
此外,来自MDPI的最新研究进一步指出,HTRA1蛋白在抗癌过程中扮演了关键角色。
研究表明,HTRA1蛋白的上调与抗癌效力密切相关。短暂的脉冲电磁场暴露能够上调HTRA1蛋白的表达,且这种蛋白对于pCM的抗癌效力是必需且充分的。
通过添加重组HTRA1蛋白,研究团队能够重现pCM的抗癌效果,而通过抗体吸收HTRA1蛋白则会阻断其抗癌效力。
这表明,HTRA1蛋白在肌肉细胞抗癌机制中具有重要作用。
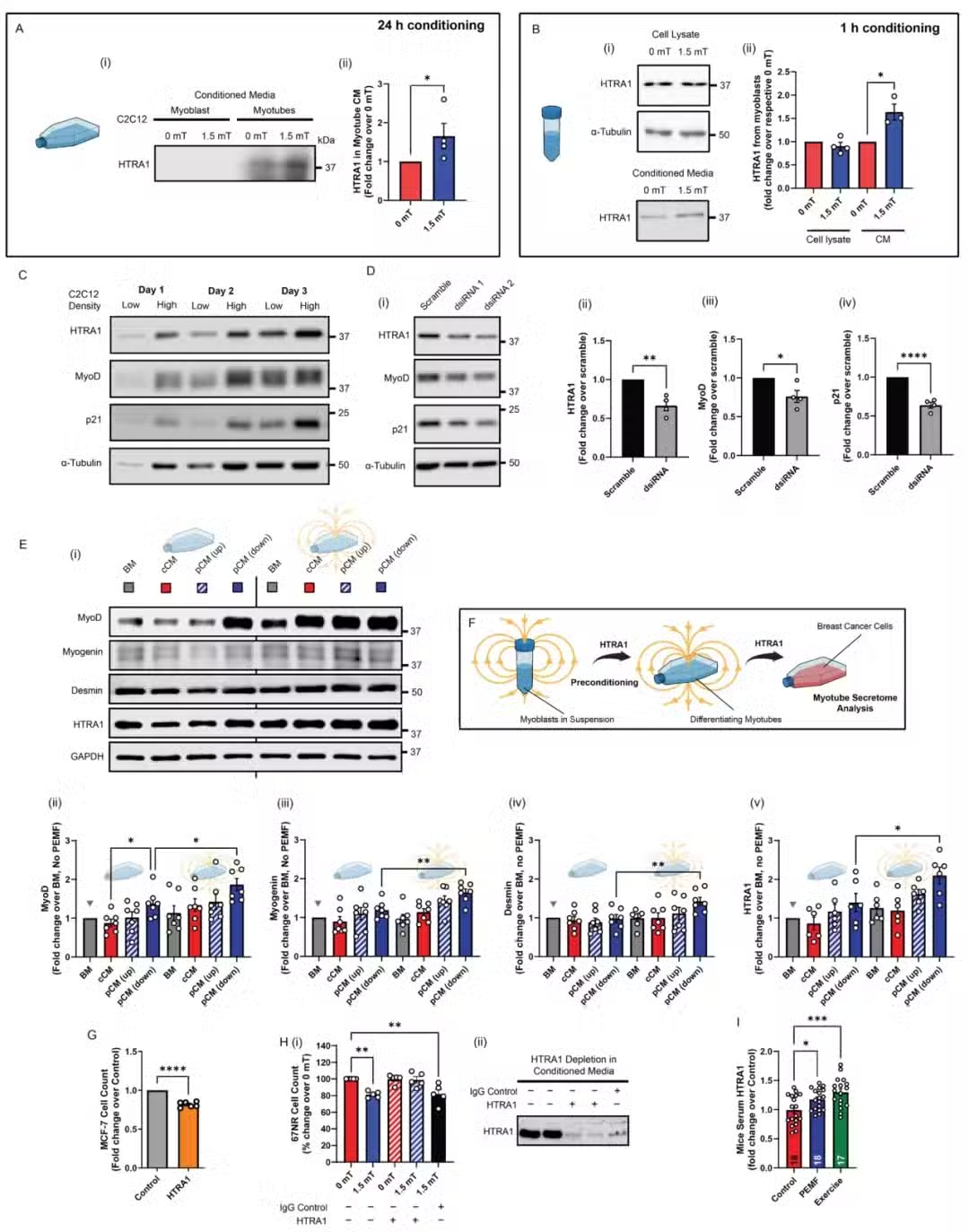
HTRA1 重现条件培养基预处理反应:HTRA1 表达在发育上重现了我们预处理范式的主要特征。重组 HTRA1 能够减弱 MCF-7 生长(图 6 G),证明了必要性和充分性,而肌管 pCM 中 HTRA1 的抗体吸收则消除了抗癌功效(图 6 H)。最后,为我们的体外预处理范式提供生理相关性,发现 HTRA1 在暴露于 PEMF 和运动的小鼠血清中上调(图 6 I),这与之前的数据一致,即类似的 PEMF 暴露可促进体外 [ 24 ] 和体内 [ 23 ] 肌肉生成。虽然基于这些实验,肌细胞分泌组的抗癌效力与 HTRA1 表达密切相关,但目前不能将其视为唯一的。
临床应用潜力
这种无药物、非侵入性的疗法不仅有望提供新的癌症治疗手段,还可能为癌症预防和早期诊断带来新的希望。
例如,许多癌症患者由于疾病的进展或治疗相关的副作用,身体状况已大幅恶化,难以承受传统的治疗方法。而这种非侵入性疗法,通过简单的脉冲电磁场处理即可激活肌肉细胞的抗癌潜能,为这些患者提供了一个安全、有效的替代方案。
研究表明,这种方法可通过肌肉分泌物的应答,利用体外和体内的脉冲电磁场进行临床利用,特别是对乳腺癌和其他癌症的治疗。
研究团队还发现,通过脉冲电磁场处理的小鼠血清也具有显著的抗癌效力,这进一步验证了这一方法的潜力。

副教授 (左)和 Tai 博士(右)证明
采用的非侵入性肌肉刺激方法可以调动抗癌防御系统
根据这项临床前研究产生的良好结果,新加坡国立大学团队正在启动临床试验,以评估肌肉靶向磁疗在人类中的抗癌潜力,并证实HTRA1对乳腺癌和其他癌症患者的抗癌作用。