NUS新加坡癌症科学研究所(CSI)助理教授Anand Jeyasekharan领导团队在了解弥漫性大 B 细胞淋巴瘤 (DLBCL) 癌症化疗后的复发方面取得了突破性进展。并在《Nature Communications》发表文章。

▲第一作者:Min Liu(新加坡癌症科学研究所)
通讯作者:Anand Jeyasekharan
DOI:10.1038/s41467-024-46220-z
新加坡国立大学 (NUS)新加坡癌症科学研究所(CSI)的研究人员在了解弥漫性大 B 细胞淋巴瘤 (DLBCL) 癌症化疗后的复发方面取得了突破性进展。
由助理教授 Anand Jeyasekharan 领导的这项研究重点关注癌症环境中发现的一种称为“巨噬细胞”的特定类型的免疫细胞,研究人员发现这些细胞的变化与患者的康复和生存程度有关。
巨噬细胞在进化上是免疫系统的一个古老的手臂,最初的进化是为了帮助吞噬入侵的微生物或垂死的细胞。它们也经常在癌症中被发现,但它们与淋巴瘤的相关性尚不清楚。
该研究的本质在于深入研究DLBCL肿瘤环境中巨噬细胞的多样性。通过采用 CSI 显微镜和多重分析 (MMA) 核心设施提供的一种称为数字空间分析 (DSP) 的新方法,该团队能够检查肿瘤中复杂的细胞混合物中巨噬细胞的分子特征,识别巨噬细胞的子集与化疗后复发有关。
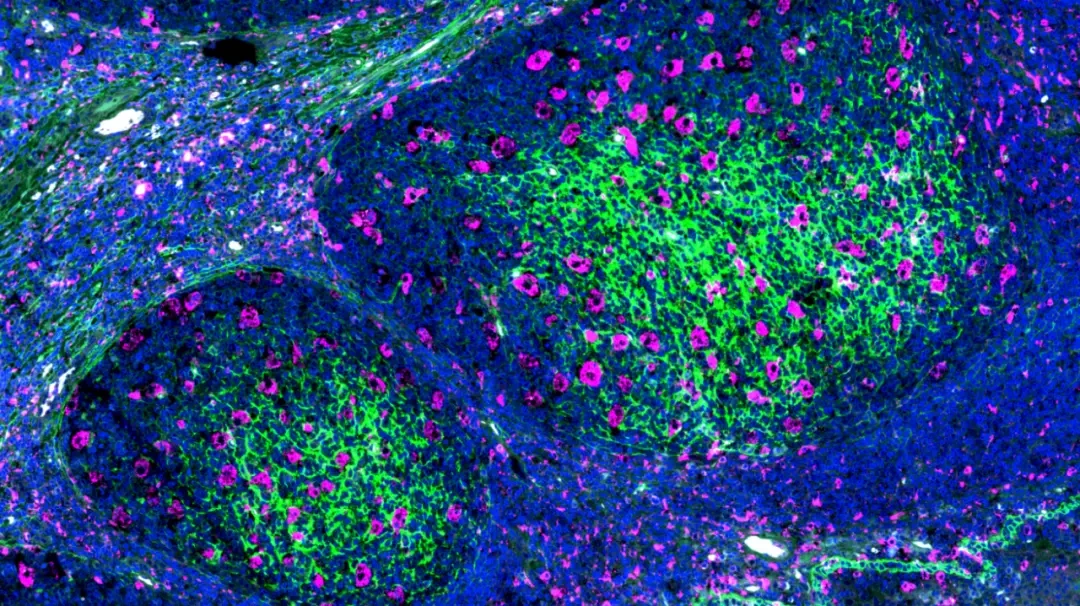
该图像显示了人类扁桃体中巨噬细胞(粉红色)的空间分布。来自 CSI 新加坡的研究人员团队发现了这些巨噬细胞的变化如何影响患者的康复和生存结果。通过识别与患者结果相关的巨噬细胞的特定模式,该研究为开发个性化治疗方法和显著改善患者护理铺平了道路,来源:NUS
这项研究展示了巨噬细胞多样性在理解和治疗这种常见形式的侵袭性淋巴瘤中的重要性,不仅可以更准确地预测疾病的进展,而且还揭示了潜在的新治疗方法。
这项研究的意义重大。由于巨噬细胞在多种癌症中很常见,因此可以使用类似的空间方法来评估与患者结果相关的巨噬细胞的独特模式。
免疫疗法被誉为癌症治疗的下一个前沿领域,目前大多数免疫治疗方法都针对另一种类型的细胞——T 细胞。对巨噬细胞多样性的深入了解有望发现新的药物和治疗方法,旨在通过对抗巨噬细胞来改变 DLBCL 和其他癌症的肿瘤环境。

Jeyasekharan 助理教授,来源:NUS
Jeyasekharan 助理教授评论道:“以前,对癌症中免疫细胞的研究是‘批量’进行的,仅提供了它们在肿瘤中存在的总体概述。然而,随着现在技术的进步,我们的团队可以以单细胞分辨率检查巨噬细胞的分子特征,同时保留其空间背景。”
他说:“我们已经确定了这些古老免疫细胞的不同特征,这有助于更准确地预测疾病的进程。这一进步为 DLBCL 的个性化分层和治疗开辟了新的可能性。”
该研究于 2024 年 3 月 8 日发表在《Nature Communications》上。
未来的工作:探索巨噬细胞在生物和临床环境中的影响
展望未来,Jeyasekharan 助理教授的团队将更深入地研究他们已确定的巨噬细胞特征的生物学和临床影响。他们的目标是了解这些特征如何影响疾病进展和患者生存。
这可能会导致新的诊断工具和治疗方案的创建,这些工具和治疗方案是根据每位患者疾病的独特特征专门设计的。这些进步不仅预示著对抗DLBCL,而且还预示著对抗其他类型癌症的新时代。
让我们来看看这个研究的实验数据吧~
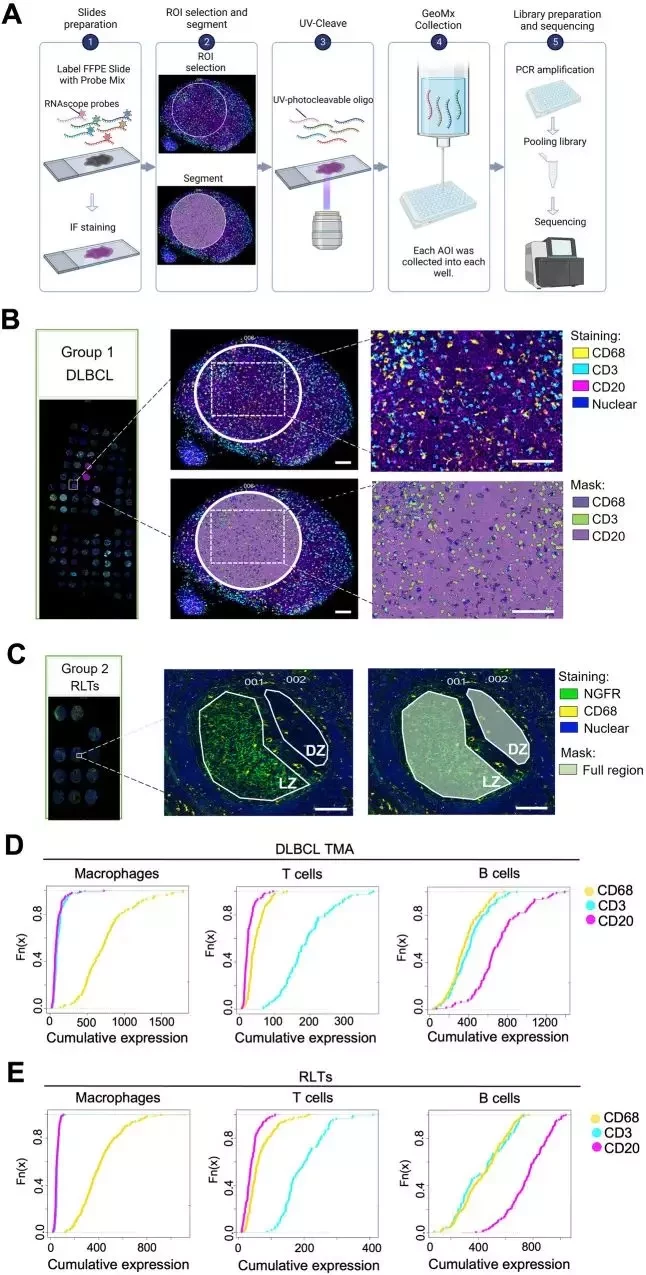
数字空间分析 (DSP) 可以从淋巴组织微区域的不同掩模中阐明一致的轮廓。GeoMx® DSP WTA 工作流程示意图(使用 BioRender.com 创建)。B、C DLBCL 组织 ( n = 87) 和 RLT ( n = 24) 的免疫萤光染色。在第 1 组中,CD68 染色的巨噬细胞(黄色)、CD3 染色的 T 细胞(青色)、CD20 染色的 B 细胞(洋红色)和 SYTO 13 染色的细胞核(蓝色)。在第 2 组中,CD68 染色巨噬细胞(黄色),NGFR 照亮 LZ(绿色),SYTO 13 染色细胞核(蓝色)。选择 ROI 后,根据染色信号对每种细胞类型进行分割,并生成相应的掩模。显示了代表性图像。比例尺:100 μm。源数据作为源数据文件提供。D、E累积密度函数显示巨噬细胞(CD68、CD163、FCGR1A和CSF1R)、T 细胞(CD3D、CD3E、UBASH3A、CD2和TRBC2)和 B 细胞(MS4A1、CD79A、CD79B、CD19、和PAX5)分别在 RLT 和 DLBCL 组织中的 CD68+ 区域、CD3+ 区域和 CD20+ 区域高度富集(Kolmogorov-Smirnov P < 0.05)。数字空间剖析,DSP;全转录组分析,WTA;弥漫性大B细胞淋巴瘤,DLBCL;反应性淋巴组织,RLT;感兴趣的区域,ROI;感兴趣的领域、AOI;福尔马林固定石蜡包埋,FFPE;亮区,LZ;暗区,DZ;神经生长因子受体,NGFR,来源:《Nature Communications》
参考文献:
Spatially-resolved transcriptomics reveal macrophage heterogeneity and prognostic significance in diffuse large B-cell lymphoma,Nature Communications(2024)