對第一劑信使核糖核酸(mRNA)冠病疫苗過敏而不能接種第二劑的人,受新加坡衛生部邀請接種科興疫苗後,將視為完成接種程序。
通訊及新聞部兼衛生部高級政務部長普傑立醫生前天(8月2日)在國會答覆工人黨阿裕尼集選區議員嚴燕松的口頭詢問時說,衛生部將安排他們到公共醫院的診所接種,以密切監測接種後的情況。
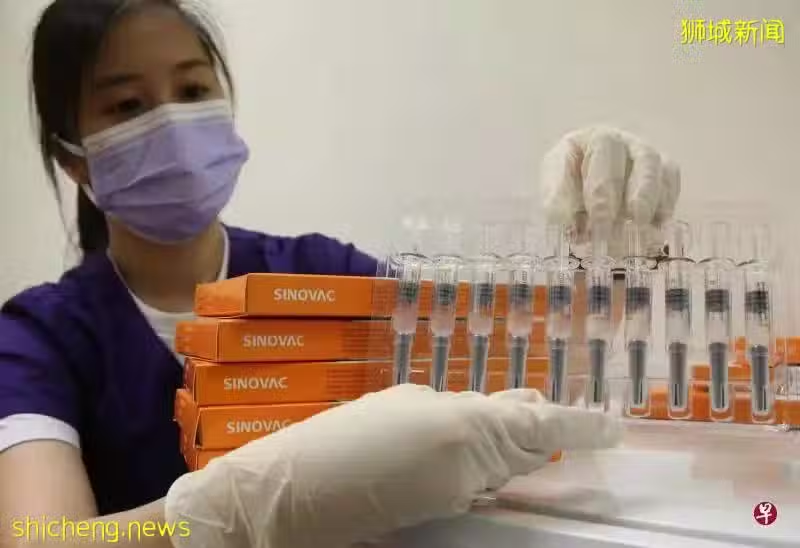
對第一劑信使核糖核酸冠病疫苗過敏而不能接種第二劑的人,受衛生部邀請接種科興疫苗後,將被視為完成接種程序。(唐家鴻攝)
據早前報道,衛生部與國家傳染病中心上月已邀請3600名對首劑mRNA冠病疫苗過敏者,參與一項名為「先信使、後科興」(Sinovac After mRNA,簡稱SAM)的計劃,免費接種兩劑科興疫苗。
受試者在接種每劑科興疫苗後的第一、第三和第七天得接受問卷調查,通報是否出現任何不良反應。
對mRNA疫苗不過敏,卻選擇自費接種兩劑科興疫苗的人,仍不算完成接種程序。這是因為科興疫苗尚未在大流行病特別採用程序(PSAR)下獲衛生科學局批准,也未納入新加坡的全國疫苗接種計劃。
不過,接種科興疫苗者日後仍可透過政府的保健資訊網(HealthHub)手機應用查看接種記錄。
就楊厝港區議員葉漢榮詢問科興疫苗的審批進度,普傑立說,科興已在7月5日向衛生科學局提交所需的關鍵數據。當局正在仔細和徹底審核數據,預計最遲在8月底完成評估。
目前,在PSAR下獲批並納入全國疫苗接種計劃的冠病疫苗,只有採用mRNA技術的輝瑞/復必泰和莫德納疫苗。
普傑立指出,對mRNA疫苗過敏者也可選擇等待美國製藥公司諾瓦瓦克斯(Novavax)生產的冠病疫苗。
新加坡今年1月和諾瓦瓦克斯簽署預購協定,購買這款採用重組蛋白技術的冠病疫苗,首批疫苗預計最遲在今年底運抵新加坡。
與mRNA疫苗不同的是,諾瓦瓦克斯疫苗採用蛋白質亞基(protein subunit)和重組病毒糖蛋白納米顆粒(recombinant nanoparticle)技術,使人體免疫系統對疫苗中的蛋白產生反應。
普傑立答覆嚴燕松的詢問時透露,衛生部與衛生科學局正同諾瓦瓦克斯密切合作,安排監管申請程序,疫苗審批進度將取決於諾瓦瓦克斯向衛生科學局提交的數據。
普傑立強調:「我們意識到及時獲取疫苗的必要,但要對疫苗的質量、安全和效能進行嚴密的科學評估,不應該有任何妥協。」
衛生部正探討為短期探訪證者打疫苗
工人黨盛港集選區議員何廷儒也詢問,抗疫跨部門工作小組是否會考慮讓那些與新加坡長期居民有密切接觸的短期探訪證持有者,在本地接種冠病疫苗。
普傑立回應時說,衛生部正在探討如何讓短期探訪證持有者接種疫苗,當中包括較弱勢者,以及因冠病旅遊限制而在新加坡長期逗留者,詳情日後公布。
記者:劉智澎
攝影:唐家鴻




