NUS由杨潞龄医学院的Ashok Venkitaraman教授领导团队,在《Cell》发表一项新研究。即使是短暂的化学反应也可能对我们的基因产生长期影响,增加癌症的风险。

▲第一作者:Li Ren Kong(新加坡国立大学癌症研究中心研究员)
通讯作者:Ashok R. Venkitaraman
DOI:https://doi.org/10.1016/j.cell.2024.03.006
新加坡国立大学(NUS)上周在一份新闻发布中宣布,其研究团队发现了新的研究成果,这些成果可能解释了长期以来不良饮食或未控制的糖尿病是如何增加癌症风险的。
在4月12日NUS表示:“这项研究获得的洞见为促进健康老龄化的癌症预防策略的进步带来了希望。”
这项开创性的研究由 Ashok Venkitaraman 教授领导,由新加坡国立大学癌症科学研究所 (CSI Singapore) 和 杨潞龄医学院下属新加坡国立大学癌症研究中心 (N2CR) 的科学家与该机构的同事共同完成科学、技术和研究 (A*STAR)。
“癌症是由我们的基因和环境因素(例如饮食、运动和污染)之间的相互作用引起的。"CSI 新加坡主任 Venkitaraman 教授说。
他认为,“这些环境因素如何增加癌症风险尚不清楚,但如果我们要采取预防措施帮助我们更长久地保持健康,了解其中的联系至关重要。”
癌细胞,来源:The Independent Singapore
研究小组对从父母那里继承了错误版本的癌症基因 BRCA2 的患者进行了研究。该基因导致他们患乳腺癌或卵巢癌的风险很高。
患者的细胞显示,它们对化学物质甲基乙二醛的作用特别敏感,这种化学物质是人体细胞分解葡萄糖以产生能量时产生的。
新加坡国立大学表示:“研究表明,这种化学物质可能会导致我们的 DNA 出现缺陷,这是癌症发展的早期预警信号。”
未遗传 BRCA2 缺陷版本但甲基乙二醛水平可能高于正常水平的个体,包括糖尿病前期或糖尿病患者,可能会表现出患癌症风险较高的相同警告信号。
糖尿病和糖尿病前期与不良饮食或肥胖有关。Venkitaraman 教授进一步解释说,通过 HbA1C 血液检测可以轻松检测到这种化学物质。
然而,更好的消息是,高甲基乙二醛水平通常可以通过良好的饮食和药物来控制,从而可以从癌细胞开始发展的时候就采取主动措施。
N2CR 的研究员、该研究的第一作者 Li Ren Kong 博士说,“我们开始这项研究的目的是了解哪些因素会增加易患癌症的家庭的风险,但最终发现了将基本能量消耗途径与癌症发展联系起来的更深层次机制。”
他发现,这些发现提高了人们对饮食和体重控制在癌症风险管理中影响的认识,
该团队的研究还提出了一种新的肿瘤形成机制,修正了长期以来关于预防癌症的特定基因的理论。
这一理论,即克努森的“两次打击”范式,可以追溯到 1971 年,并提出在癌症出现之前,细胞中的基因需要永久失活。
然而,新加坡国立大学的研究小组发现甲基乙二醛可以暂时灭活预防癌症的基因。这表明,随着时间的推移,反复不良饮食或不受控制的糖尿病可能会“叠加”,从而增加患癌症的风险。

国大属下新加坡癌症科学研究所所长文基塔拉曼教授说:“癌症是由我们的基因与饮食、运动和污染等环境因素相互作用引起的。”,来源:联合早报
新加坡国立大学写道:“这一新知识可能会对改变该领域未来的研究方向产生影响。”并补充说,该团队的重要发现于 2024 年4 月 11 日发表在生物医学研究领域最具影响力的科学期刊之一《Cell》上。
NUS还表示,团队的下一步研究涉及了解“糖尿病或不良饮食等代谢紊乱是否会影响新加坡和其他亚洲国家的癌症风险”。
让我们来看看这个研究的实验数据吧~
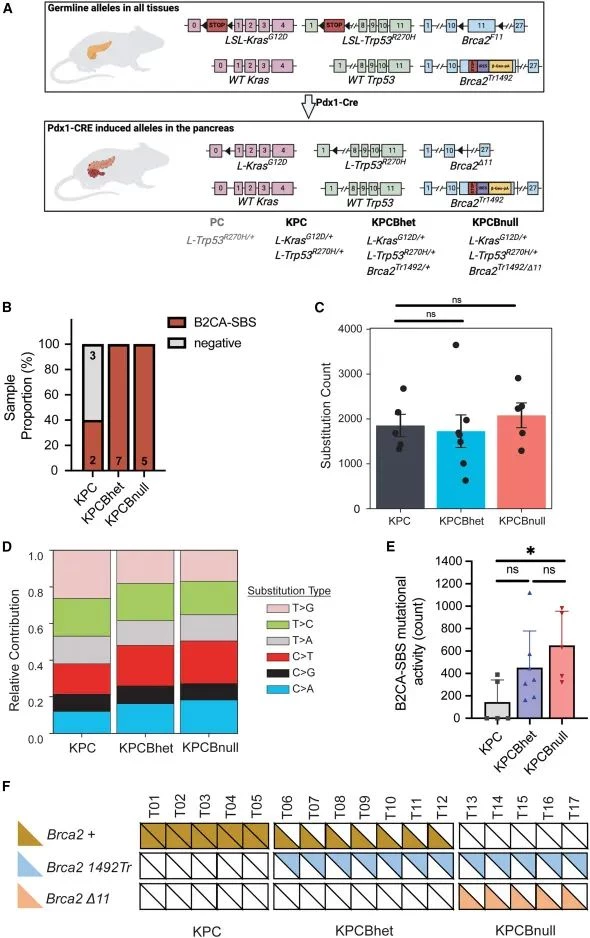
(A)胰腺中不具有 (KPCBhet) 和具有 (KPCBnull) 组织限制性 CRE 介导的Brca2外显子 11 缺失的靶向等位基因。Brca2 Tr1492等位基因模拟所有体细胞组织中种系Brca2杂合性。
(B) 来自 KPC (n = 5)、KPCBhet (n = 7) 和 KPCBnull (n = 5) 肿瘤的 PDAC 细胞系中 B2CA-SBS 特征的普遍性。
(C) 从 (B) 中的基因组中提取的总替换计数。条形图代表平均值±SEM。
(D) 来自所示遗传背景的 PDAC 细胞系的碱基取代谱。
(E) 来自指定遗传背景的 PDAC 细胞系中的 B2CA-SBS 活性。条形图代表平均值+SD。
(F) (B) 中使用的 PDAC 细胞系中的Brca2基因型。1492Tr代表Brca2 nt4668-4989缺失;Δ11,Brca2外显子 11 缺失。使用集成基因组查看器 (IGV)从 WGS确定Brca2基因型。
,来源:《Cell》
参考文献:
A glycolytic metabolite bypasses “two-hit” tumor suppression by BRCA2,Cell(2024)
























